问题1、2回答:
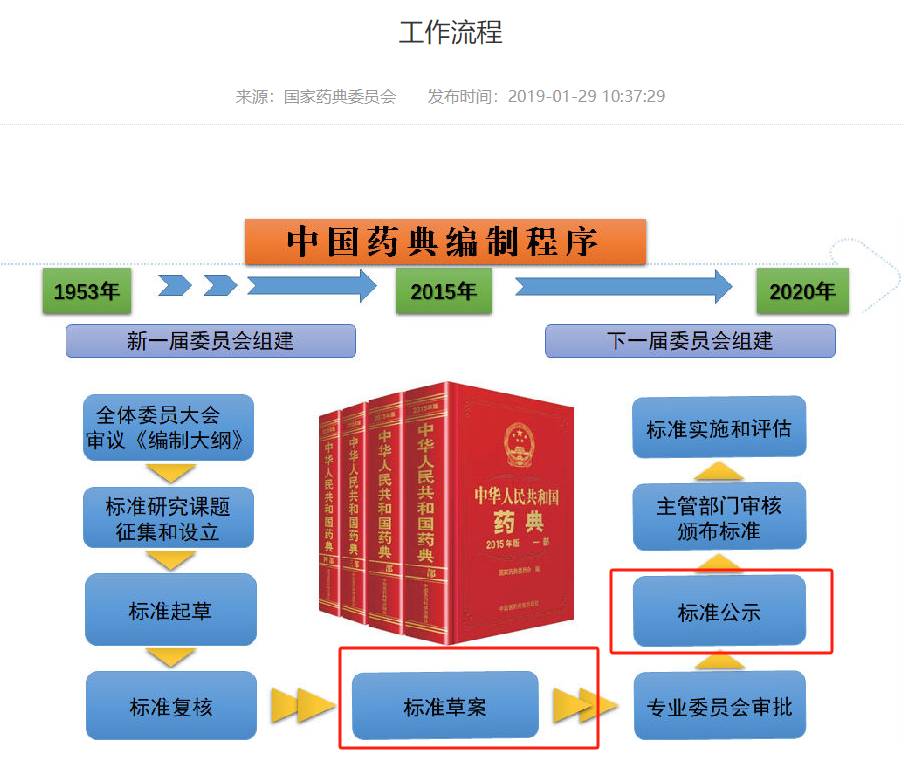
药典编制官方程序如下图,且标准草案的公示明确:“拟修订《中国药典》9101分析方法验证指导原则”“公示期满未回复意见即视为对公示标准草案无异议”,故流程上通则9101会在2025版药典中更新,但不一定与目前草案完全一致(但大概率不会更改太多);目前该标准只是草案尚未正式执行,仍可按照2020版药典进行执行;
问题3回答:
草案提出的“可采用预测区间、容忍区间或置信区间来评价联合的准确度和精密度”来源自ICH Q2(R2)(其实草案的《9101分析方法验证指导原则修订说明》也说明了来源),如何确定可参考该文件的附件2:分析技术的说明性示例:
3.3.3准确度和精密度的合井评价方式
替代单独评估准确度和精密度的方法是考虑二者的总体影响,通过一个合并的性能标准进行评估。
方法开发期间生成的数据可能有助于确定最佳方法,并确定适当的性能标准,用于合并的准确度和精密度的评估。可使用预测区间、容许区间或置信区间来评价合并的准确度和精密度。如果合理,其他方法也可以接受。
供参考,谢谢~
感谢回答。
对于问题3我想问的是在报告准确度或者精密度的时候,我是报告置信区间还是报告预测区间,或者是容许区间?
另外想新增个问题,对于置信区间,应该如何确定α的值?
(一)草案中已有的描述:
【准确度和精密度可以分别进行评价,它们各有预定义的可接受标准。将这两个性能特征联合验证是评价分析方法适用性的另一种方法。】
①分别评价:
准确度:【准确度试验结果应报告为在试样中已知添加量分析物的平均回收率,或报告为平均值与可接受真值之间的差值,同时提供合理的100(1-α)%置信区间(或其他合理的统计区间),除另有合理的证明,所提供的置信区间应与对应的准确度可接受标准相匹配。】,建议用置信区间,其他统计方式只要自我评估合理就行;
精密度:【所有的精密度试验都应报告标准偏差、相对标准偏差(变异系数),和适当的100(1-α)%置信区间或其他合理的统计区间。除另有合理的证明,置信区间应与对应的精密度可接受标准相匹配】,建议用置信区间,其他统计方式只要自我评估合理就行;
②联合验证:
【可采用预测区间、容忍区间或置信区间来评价联合的准确度和精密度】,即没有明确规定用哪种方式进行评价,是需要自行结合实际评估的;
(二)置信区间:
引用吹口琴的猫老师的文章:
【置信区间(CIs)是统计学中的一个关键概念,特别是在制药领域,结果需要可靠和准确。置信区间是一个范围,其中未知参数(如总体平均值或比例)可能在一定的置信水平下落入该范围。置信区间用于量化从样本数据得出的估计值的不确定性。】
【置信区间是通过将误差范围加减到样本估计值来构造的。误差范围由所需的置信水平(通常为95%或99%)和数据的可变性决定】
【 置信区间(CI)是一个值范围,用于估计总体参数(如均值或比例)在某个置信水平下可能落入的范围。它用于表示与样本统计量相关的精确性和不确定性,样本统计量是从数据样本中得出的。置信区间越宽,对真实总体参数的不确定性就越大。】
【置信水平,另一方面,是置信区间包含真实总体参数的概率。它通常表示为百分比,如95%或99%。95%的置信水平意味着,如果我们多次重复抽样过程,并为每个样本计算置信区间,那么大约95%的区间将包含真实的总体参数。 】
所以, 置信水平取多大,取决于具体情况,以及对区间中包含总体平均值这一说法有多大信心。置信水平越高,区间越宽,置信区间包含总体平均值的概率也就越大。常用的置信水平为95%。
而根据现行版药典(2020版)通则9101:
准确度:【置信区间(置信度一般为95%)】,即α取了0.05,置信度(置信水平)为100(1-0.05)%=95%;
而根据目前的草案而言,不再明确“置信度一般为95%”而以“100(1-α)%”代替,这个α有了更多的可操作空间,合理即可。
关于统计学的问题,目前只了解到这里,如有错误请指正,观点仅供参考。
这{{threadTextType}}正{{isAdminText}}
为帮助审核人员更快处理,请填写举报原因:
为帮助审核人员更快处理,请填写举报原因:
