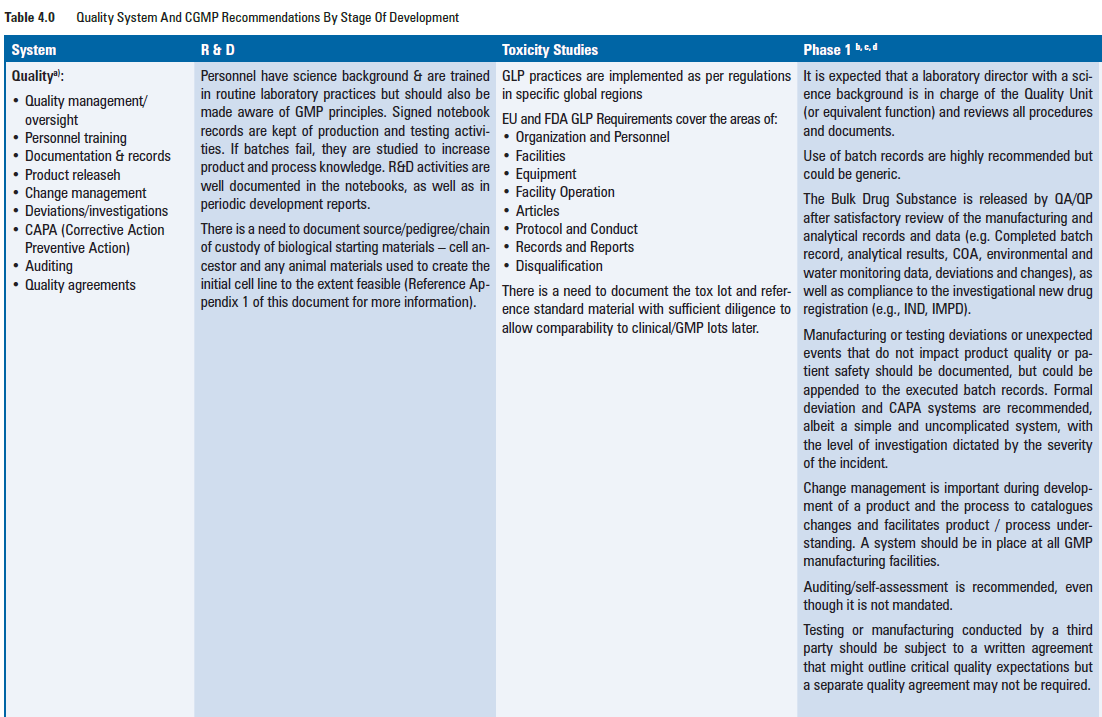
想咨询下研发的记录设计和生产的记录设计相比可经弱化到什么程度
QA
比如:生产的记录我们要求必须有经批准的原版,必须有编号和版本号,然后从原版复印来使用,同一个记录不管有多少个复印件都是相同的编号和版本号,只不是额外加盖一个不同的受控号。
补充一下,实验记录是空白的记录本,主要是指质量管理相关的记录, 比如仪器使用记录, 培训记录,标准品使用台帐等这些。
5个回答
评论
匿名
提交
取消
匿名
{{item_parent.created_at}}
置顶
批准
驳回
编辑
等待审核
已驳回
回复
{{item_parent.show_reply_list ? '收起回复' : '查看回复'}}({{item_parent.children.length}})
编辑
提交
取消
写回复
匿名
提交
取消
{{item_children.from_user}} 回复 {{item_children.to_user}}
{{item_children.created_at}}
批准
驳回
编辑
等待审核
已驳回
回复
编辑
提交
取消
写回复
匿名
提交
取消
这{{threadTextType}}正{{isAdminText}}
举报
提交
取消
为帮助审核人员更快处理,请填写举报原因:
举报
提交
取消
为帮助审核人员更快处理,请填写举报原因: