无菌药品灯检后的AQL抽检疑问?
QAQC生产管理处方与工艺
问题1.如图中文字所述,生产进行的100%灯检后,合格的灯检后样品需要被AQL抽检进行灯检效果的再确认,而AQL抽检是按照三种缺陷不同的拒绝概率的(参照gb2828-2012)),假设产品批量是15w支,按照一般检验水平III的等级,样本量字码是P,800支,是每种缺陷都 分别抽800支,抽三次对应三个缺陷的抽样量,还是一次性共抽800支,如果是一次性共抽800支这种情况下,严重缺陷的数量会被累计至一般缺陷样本数量里面吗?
问题2.在使用全自动灯检仪器前需要进行阳性的测试,阳性的是各种大于50um的可见异物,从50um至2000um,生产端既如此严格了,为什么到了QC端,合格标准却变成了mm级别(药典中0904结果判断中的2mm))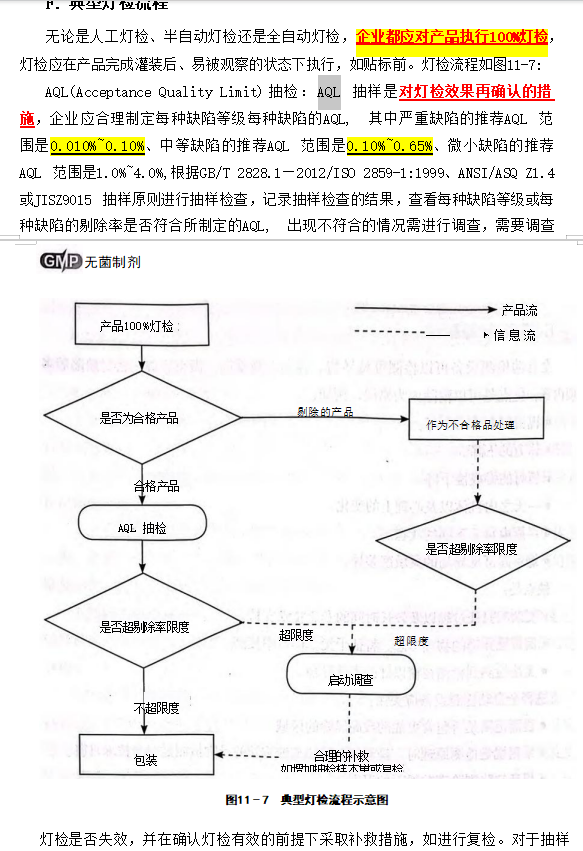
3个回答
评论
匿名
提交
取消
匿名
{{item_parent.created_at}}
置顶
批准
驳回
编辑
等待审核
已驳回
回复
{{item_parent.show_reply_list ? '收起回复' : '查看回复'}}({{item_parent.children.length}})
编辑
提交
取消
写回复
匿名
提交
取消
{{item_children.from_user}} 回复 {{item_children.to_user}}
{{item_children.created_at}}
批准
驳回
编辑
等待审核
已驳回
回复
编辑
提交
取消
写回复
匿名
提交
取消
这{{threadTextType}}正{{isAdminText}}
举报
提交
取消
为帮助审核人员更快处理,请填写举报原因:
举报
提交
取消
为帮助审核人员更快处理,请填写举报原因:
