5个回答
1. 制剂除菌过滤前的微生物限度≤10 cfu/100 mL在下面的监管机构指南或行业指南都还可以找到:
A. NMPA《除菌过滤技术及应用指南》;
C. USP<1119> Bioburden Monitoring Table 3. Recommended Bioburden Limits
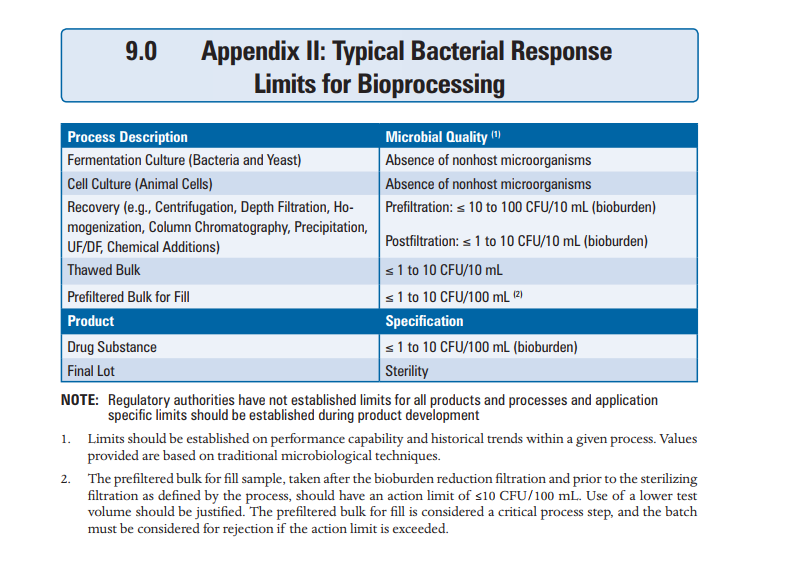
D. PDA TR69 Section 9.0 Appendix II Typical Bacterial Response Limits for Bioprocessing
2. 原液如果是经过除(减)菌过滤后的最终原液,并且在制剂最终除菌过滤前无其他微生物负载降低手段,通常也要求≤10 cfu/100 mL。
3. 在上述B和D中分别提到“Due to limited availability of the formulated medicinal product, a pre-/filtration volume of less than 100 ml may be tested if justified.” “Use of a lower test volume should be justified.” 可以参考这篇文章:A Risk-based Approach to Setting Sterile Filtration Bioburden Limits 。
评论
匿名
提交
取消
匿名
{{item_parent.created_at}}
置顶
批准
驳回
编辑
等待审核
已驳回
回复
{{item_parent.show_reply_list ? '收起回复' : '查看回复'}}({{item_parent.children.length}})
编辑
提交
取消
写回复
匿名
提交
取消
{{item_children.from_user}} 回复 {{item_children.to_user}}
{{item_children.created_at}}
批准
驳回
编辑
等待审核
已驳回
回复
编辑
提交
取消
写回复
匿名
提交
取消
这{{threadTextType}}正{{isAdminText}}
举报
提交
取消
为帮助审核人员更快处理,请填写举报原因:
举报
提交
取消
为帮助审核人员更快处理,请填写举报原因: