9个回答
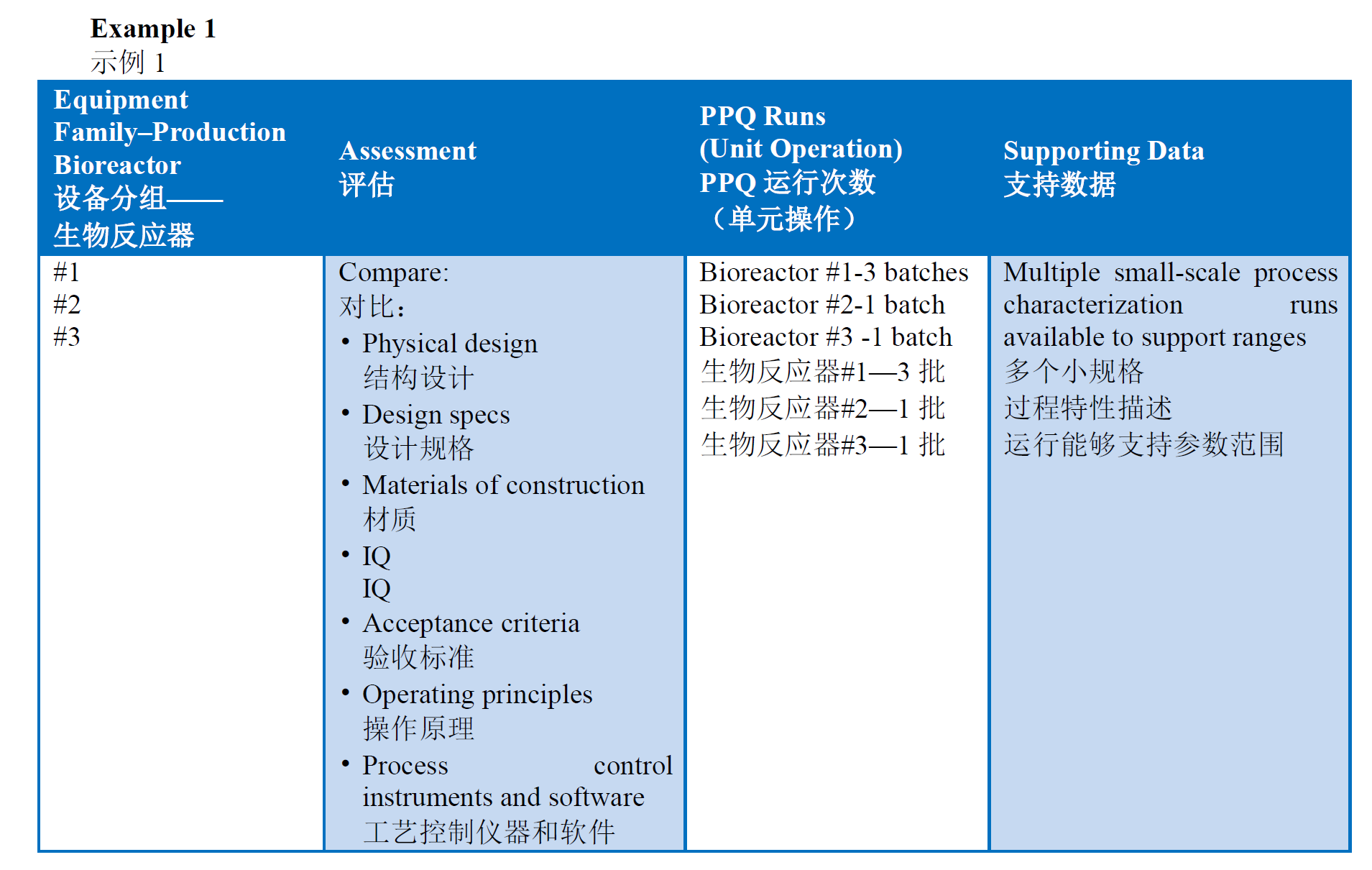
上游工艺的细胞培养通常会使用多个等同的设备, 因此在验证过程中需依据风险评估采用分组法,制定合理的验证批次数。参考《药品GMP指南-无菌制剂-下册》(2023年版)中表4-10《分组法进行多个生产生物反应器 PPQ 示例》相关备注:
注:①工艺验证可采用同一个反应器连续3批, 其他反应器各1批的验证策略, 如需减少验证批次数应进行充分风险评估, 例如对于完全相同的生物反应器且已进行过多批次商业化生产的生产线, 可以基于设备的等同性评估、 已掌握的工艺知识、 积累的平台经验、 相关设施设备设计(公用工程、 反应器的结构设计、 工艺控制仪器及软件等)及已完成的相关确认(如IQ、 OQ 等)等方面综合评估合理制定验证批次数, 但多个相同反应器一起验证的总批次应不少于3批。 ②表4-10示例中“批次” 指全工艺步骤进行的验证活动, 并非针对某一反应器或某一步骤单独展开验证。
因此建议三个相同型号生物反应器基于相关设施设备设计(公用工程、 反应器的结构设计、 工艺控制仪器及软件等)及已完成的相关确认(如IQ、 OQ和PQ),若有足够的工艺知识、 积累的平台经验,比如多批次商业化生产可比数据,可以跟监管机构进行沟通,做工艺验证的时候每个罐做一批,同时基于药品生命周期原则进行持续工艺确认和回顾。
评论
匿名
提交
取消
匿名
{{item_parent.created_at}}
置顶
批准
驳回
编辑
等待审核
已驳回
回复
{{item_parent.show_reply_list ? '收起回复' : '查看回复'}}({{item_parent.children.length}})
编辑
提交
取消
写回复
匿名
提交
取消
{{item_children.from_user}} 回复 {{item_children.to_user}}
{{item_children.created_at}}
批准
驳回
编辑
等待审核
已驳回
回复
编辑
提交
取消
写回复
匿名
提交
取消
这{{threadTextType}}正{{isAdminText}}
举报
提交
取消
为帮助审核人员更快处理,请填写举报原因:
举报
提交
取消
为帮助审核人员更快处理,请填写举报原因: