一、URS介绍
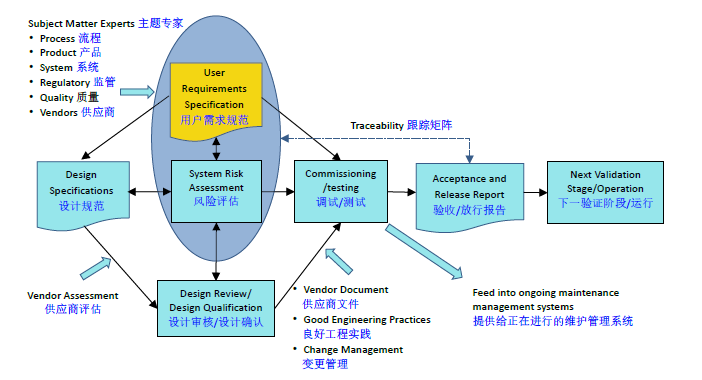
ISPE调试与确认第二版2019年发布的指南中,把User Requirements Specification(URS)放在一个重要的位置。在该指南中认为URS汇集了来自多学科资源的系统需求,以支持系统设计、C&Q、操作和维护。在C&Q 流程中,它是一个基本文档,用于识别系统的产品和流程要求。这些与产品质量相关的用户需求是基于产品知识(CQAs)、流程知识(CPP),监管要求和组织/现场的质量要求。URS 中产品和流程要求是 C&Q 流程的输入;它们提供了基于科学的知识,形成了将QRM 应用于C&Q 的基础。
现基本上的做法都是为直接影响熊起草URS,在ISPE C&Q中建议为每个可能影响产品质量的系统或者直接影响系统开发URS。但是URS的表现形式可以是多样的,并非所有的均需要形成正式的URS(如后文模板),URS的表现形式可以是采购申请、功能规范、变更请求或数据表。对于标准的或现成或简单的设备,系统的URS内容可能仅是一个采购订单,或者供应商的产品介绍单。
无论URS的表现形式是什么,系统的验证都是根据需求进行验证的。
URS应用可验证的术语说明需求,不需描述如何满足及无法核实的参数。应描述项目的背景和系统的预期用途、描述需求类别和需求来源,还需包含数据完整性要求、数据存储和显示要求、报警要求、自动化要求。
需求的类别可以有:质量、商业、HSE、过程要求、自动化和记录、设计和建造、操作与维护、其它,如果类别不适用可输入"不适用“。这里之所以分类是为了让需求更清楚,哪些是质量关键必需满足的,哪些不是。这里可以简单的分类,法规和影响质量需求的内容就可以是划为质量类、商业类的为可能涉及到费用或者期望达到的。
需求的来源一般有:产品和工艺知识、GMP法规要求、质量控制要求、风险评估、受控的参数范围和精度、区域和场地要求、HSE及系统所有者的需求、工程和行业规范需求。
以下URS模板是将URS与合同中的商业要求完全分开,对于C&Q中,他给出的模板是一个纯粹站在用户的角度提出的一个URS,但是在实际的执行过程中,往往URS中没有提出的需求,在合同中容易遗漏,因为这是两个部门执行的事情,需求部门是一个团队,采购合同部门又是一个团队,所以我个人建议还是将一部分需求纳入到URS中,比如文件的需求,可以划为其它类型中。
URS名称、编号、版本号
URS审批页
|
列表 |
姓名 |
部门 |
签字/日期 |
|
使用部门起草 |
张三 |
生产部 |
|
|
。。。。 |
。。。。。 |
|
|
|
相关部门审核 |
李四 |
工程设备部 |
|
|
李五 |
质量部 |
|
|
|
。。。。 |
。。。。 |
|
|
|
批准 |
张六 |
生产部 |
|
正文
1目的和范围:确定URS将涵盖的系统
2术语和缩写
2.1术语
|
术语 |
定义 |
|
|
|
|
|
|
|
|
|
2.2缩写
|
缩写 |
定义 |
|
|
|
|
|
|
|
|
|
3.参考
|
编号 |
名称 |
|
|
|
|
|
|
|
|
|
4.系统概述
提供一个简单的系统描述并展示它如何与其他系统接口。如适用,列出输入和输出。
可参考适当的工艺流程图、数据流程图、网络图等。
如有必要,列出管道和仪表图,以明确定义用户要求的范围。
下表定义了XXX系统的用户需求。每一个表格都包含用户对某一功能领域或专业的需求,如工艺、设计和施工、操作和维护等。
自动生成的唯一需求号、
要求 、
类型(下拉菜单,允许选择质量、EHS或业务或其他作为属性类型,确定哪些是质量关键必需的,哪些不是)、
来源(项目要求文件、产品和工艺知识/GMP法规要求/质量控制要求、风险评估、受控的参数范围和精度、区域和场地要求、HSE及系统所有者的需求、工程和行业规范需求)。
5.1.
工艺与技术参数
|
编号 |
要求内容 |
类型 |
来源 |
|
URS5.1-1 |
系统的包装能力不低于50-80袋/分钟。 |
业务 |
项目 |
|
URS5.1-2 |
料仓体积不小于500升 |
业务 |
项目 |
|
URS5.1-3 |
该设备将能够处理具有以下关键物理特性的一系列临床产品。 密度:0.9-1.2g/ml 粘度:1-20 cP 表面张力 25-65 mN/m |
质量 |
产品工艺 |
|
URS5.1-4 |
基于 20 土 2°C 时的水,最大剪切速率为 122 000 s-1 |
质量 |
产品工艺 |
|
URS5.1-5 |
装量进度应符合中国药典袋装颗粒剂要求 |
质量 |
质量标准 |
5.2.
材质与加工制造要求
|
编号 |
要求内容 |
类型 |
来源 |
|
URS5.2-1 |
AII 产品接触弹性体和垫片材料应为制药级且符合 USP Sec <88> V1 类和 CFR 177.2600 类。 |
质量 |
质量标准 |
|
URS5.2-2 |
生产产品接触材料不得与产品或以下清洁溶液反应、添加剂或吸收:x、y 和 z,以改变产品质量。 |
质量 |
GMP设备章节 |
|
URS5.2-3 |
设备必须具有卫生设计、光滑、清洁、防不透、无反应、无添加剂和耐清洗/消毒剂 |
质量 |
GMP设备章节 |
5.3.
自动化和记录
|
编号 |
要求内容 |
类型 |
来源 |
|
URS5.3-1 |
每个授权用户必须具有唯一的用户 ID 和关联的密码 |
质量 |
21 CFR 第 11 部分 |
|
URS5.3-2 |
自动化系统应提供用于配置、分类、确定优先级、日志记录、通知、显示、确认、禁用和报告警报和事件的工具和实用程序 |
业务 |
项目 |
|
URS5.3-3 |
设备能自动生成报告,并可对接SCADA系统打印 |
业务 |
项目 |
|
URS5.3-4 |
断电后数据不得丢失 |
|
|
5.4.
EHS要求
|
编号 |
要求内容 |
类型 |
来源 |
|
URS5.4-1 |
设备产生的噪声水平应小于 75 dBA |
业务 |
EHS要求 |
|
URS5.4-2 |
应具有硬接线紧急停止,在触发时立即关闭并释放所有存储的能量。 |
业务 |
EHS要求 |
|
URS5.4-3 |
系统必须能够从UPS电源运行,当断电时可自动切换。 |
业务 |
项目 |
5.5.
公用工程
|
编号 |
要求内容 |
类型 |
来源 |
|
URS5.5-1 |
用水在 5 bar处可用。 |
N/A |
公用工程设计 |
|
URS5.5-2 |
场蒸汽在 6 bar 处可用 |
N/A |
公用工程设计 |
|
URS5.5-3 |
240/380 V 50 Hz,安装时最大额外消耗为 800
kW。 |
N/A |
公用工程设计 |
5.6.
操作维护
|
编号 |
要求内容 |
类型 |
来源 |
|
URS5.6-1 |
操作 SOP 应包括设备使用前检查叶轮密封的要求。 |
质量 |
风险评估 |
|
URS5.6-2 |
操作性 SOP 应包括高温报警时所需操作的定义 |
质量 |
风险评估 |
6.
变更
|
变更内容 |
变更原因 |
|
|
|
注:QRM:质量风险管理
为帮助审核人员更快处理,请填写举报原因:
为帮助审核人员更快处理,请填写举报原因:
